


Universidad Central del Ecuador
Facultad de Filosofía, Letras y Ciencias de la Educación
Carrera de Pedagogía de las Ciencias Experimentales Química y Biología


AGUA
La sustancia más abundante en los seres vivos
El agua es la sustancia más abundante en los seres vivos, ya que constituye alrededor del 70 % de su masa. Debido a su estructura molecular, presenta propiedades que la hacen imprescindible para el desarrollo de
la vida.

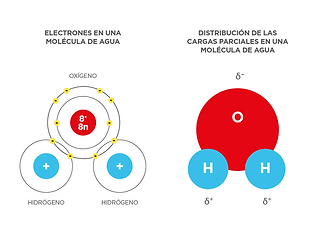

Estructura molecular
La molécula de agua (H2O) está formada por el enlace covalente entre un átomo de oxígeno y dos de hidrógeno, y se caracteriza por:
Compartición de dos electrones: La compartición de electrones permite manteneruna coniguración estable.
Polaridad de la molécula: El oxígeno es más electronegativo que el hidrógeno, por lo que atrae hacia su núcleo a los electrones del hidrógeno.
Formación de puentes de hidrógeno: La atracción entre los átomos de hidrógeno y de oxígeno de diferentes moléculas de agua debido a su diferencia de carga forma un tipo de enlace débil que lo conocemos como puente de hidrógeno.
Bioelementos
Propiedades fisicoquimicas
Gracias a su composición y estructura molecular, el agua presenta unas propiedades fisicoquímicas que la convierten en una sustancia indispensable para la vida. A continuación, veremos las principales propiedades isicoquímicas del agua y su utilidad para los seres vivos:
• Elevada tensión supericial: la fuerte cohesión entre las moléculas de agua, causada por los puentes de hidrógeno, provoca que el agua tenga una elevada tensión supericial.
• Capilaridad: Este fenómeno consiste en el ascenso del agua sin gasto energético a través de tubos estrechos.
• Elevado calor especíico: La capacidad caloríica especíica, es decir, la cantidad de calor necesaria para aumentar 1 °C la temperatura de un kilogramo de una sustancia, es de 1 caloría/gramo · °C, o lo que es lo mismo: 4186 julios/ gramo.
• Gran poder disolvente: debido a la polaridad de las moléculas, el agua tiene la capacidad de disolver distintas sustancias ya sean iónicas o polares.
• Densidad: el valor máximo de densidad del agua se obtiene a 4 °C, cuando se establecen numerosos puentes de hidrógeno entre sus moléculas. En este punto, consideramos la densidad del agua como 1 kg/dm3, o lo
que es lo mismo, cada litro de agua tiene una masa de un kilogramo.
• Bajo grado de ionización: por lo general, solo una pequeña proporción de las moléculas de agua tienden a ionizarse, es decir, uno de los átomos de hidrógeno se separa para combinarse con otra molécula de agua y esto da lugar al ion hidronio (H3O+) y al ion hidroxilo (OH–).


